食管癌是我国常见的恶性肿瘤,发病率居第6位,死亡率居第4位,是严重危害人民健康的重大疾病之一。为了更好地提高食管肿瘤的诊治水平,加强对食管肿瘤的预防,南京医科大学第一附属医院刘连科教授、北京大学肿瘤医院鲁智豪教授组织编写了《实用食管肿瘤诊疗学(第2版)》。第2版对第1版的内容进行了全面修订,更多地引用循证级别高的文献资料和研究进展,增加了食管癌多基因检测、循环肿瘤细胞检测、食管癌的免疫药物治疗(抗体类)等内容。
专著在第十章对食管癌的循环肿瘤细胞检测做了详细介绍。循环肿瘤细胞(CTC)是指在肿瘤原发灶或转移灶形成或增长过程中进入外周血循环系统的肿瘤细胞,CTC具有不同的细胞分型:单个CTC、CTM、中性粒细胞CTM,其中CTM的侵袭性远大于单个CTC,转移潜能比单个CTC高23-50倍,而中性粒细胞CTM具有驱动细胞周期进展和增加CTC转移的潜能,会导致更高的肿瘤转移风险。
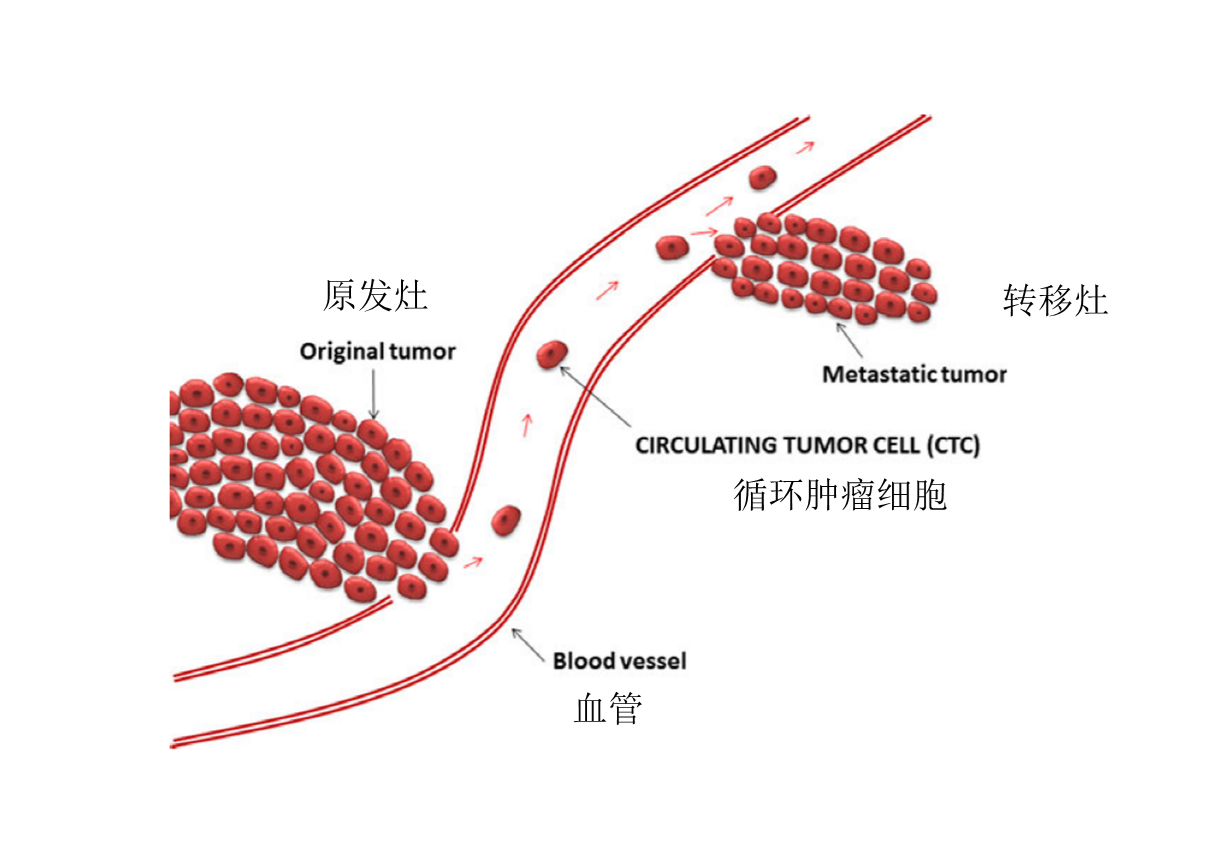
图10-1 CTC在体内形成的过程
在临床应用方面,CTC可用于食管癌复发诊断、疗效评估及预后判断。多项研究显示,CTC与食管癌(ESCC)临床特征及患者预后相关,与临床分期和新辅助化疗疗效相关,CTC计数变化可用于预测无进展生存率,治疗前后CTC数量的动态变化可能作为预测临床疗效的指标。
CTC富集方法有很多,如免疫亲和法、梯度离心法、介电电泳法、过滤法、体内富集法等。目前临床检测CTC主要有两种,分别基于细胞表面标志物(如CellSearch)和细胞大小差异(ISET)进行CTC分离,多项研究显示ISET技术(以CTCBIOPSY为代表)敏感度高于CellSearch系统(32.8% vs 1.6%),且CTCBIOPSY方法可兼容下游的各种细胞分析和鉴定技术,具有更好的应用前景。对于捕获的CTC,可以从细胞的蛋白质、DNA、RNA等方面进行分析,探寻肿瘤进展的相关机制,实现肿瘤的个体化治疗。

图10-3 CTC在个体化治疗中的意义
此外,专著在第十章第四节以CTCBIOPSY系统为例详细介绍CTC检测流程,先通过8μm孔径纳米微筛富集血液中的肿瘤细胞,然后对获取的细胞进行细胞形态学鉴定。
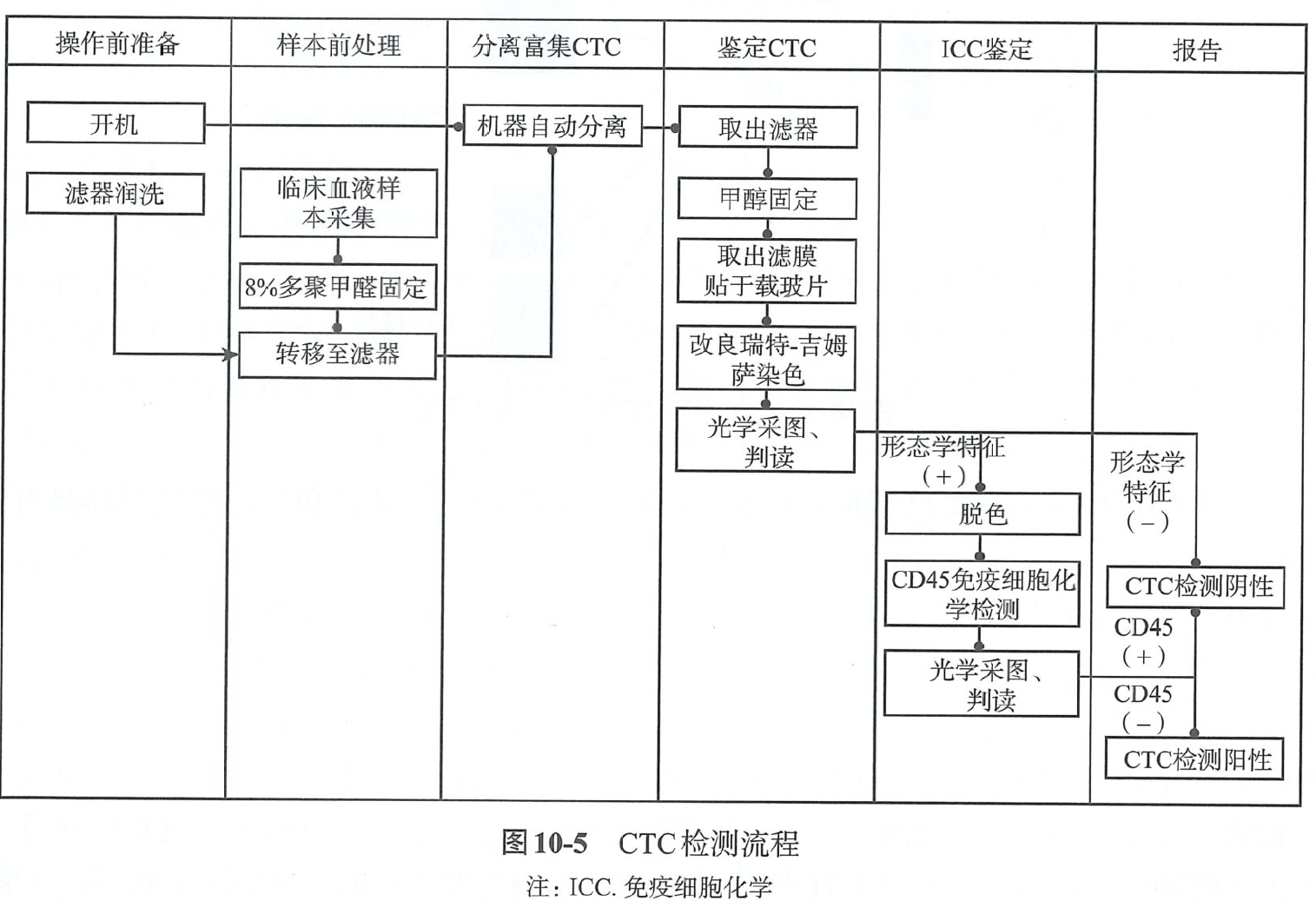
CTCBIOPSY系统为芝友医疗自主研发的CTC分离系统,在2015年国内首家获得NMPA批准的CTC分离设备注册证,目前已经在国内100多家三甲医院进行临床应用,收录进入《实用现代病理学技术》、《神经系统肿瘤》和《CACA技术指南-液体活检》临床指南。为推动CTC检测的规范及标准化发展,芝友医疗联合国内临床专家在结直肠癌(2018)、肝癌(2019)、食管鳞状细胞癌(2019)及胃肠道肿瘤(2023)领域已发表了4篇CTC临床专家共识,为CTC检测树立了行业标准。

附录《实用食管肿瘤诊疗学》(第2版)编写名单: