个体化用药是精准医学的发展趋势,可以打破以往千人一药的方案,通过遗传分析,给出个体化的指导,不仅能够加快治疗进程缓解患者身体的痛苦,同时也减轻了患者经济上的负担。
根据2021年3月份发布的国家不良反应年度检测报告显示2020年全国共收到167.6万份《药品不良反应/事件报告表》,从1999年到2020累计收到1687万份,报告显示从1999年到2020年全国药品不良反应/事件报告数量呈增长趋势,因此无法预计的个体差异严重影响了用药的安全及效率!
药物基因组学在精准医学的应用越来越广泛,研究发现,多种常见处方药物(如他汀)在人体内的代谢与若干个基因密切相关。基因不同,机体对特定药物的代谢能力不同,从而直接关系到药物的疗效和毒副作用:若药物在体内代谢较慢,代谢产物不易排出体外,容易积聚而引起药物性肝炎,严重者则引起药物中毒;若药物在体内代谢过快,就会导致常规剂量疗效降低或者无效,延误病情,但是盲目地增加剂量又容易导致用药过量引起的药物性肝炎或药物中毒,因此精准服用药物至关重要。

由于他汀的用药人群非常广泛,覆盖的科室众多,比如心内科,神内科,老年科,内分泌科等,并且患者长期服药,所以它的安全性、有效性尤为重要,2013年HPS2-THRIVE研究分析了中国人和欧美人对于他汀发生副作用情况,结果显示中国人服用他汀出现副作用风险比欧美人高10倍[1];因此对于他汀相关的药物基因组研究已经非常成熟了; 目前研究比较多的相关基因有SLCO1B1和APOE,这两个基因缺一不可,SLCO1B1与他汀的安全性相关[2-4],APOE与他汀的有效性相关[5-7]。
其实SLCO1B1和APOE这两个基因的影响远超于此,对其他药物的影响也是非常显著的, CPIC指南和PharmGKB上都有有明确的推荐,如下表所示[7-8]:
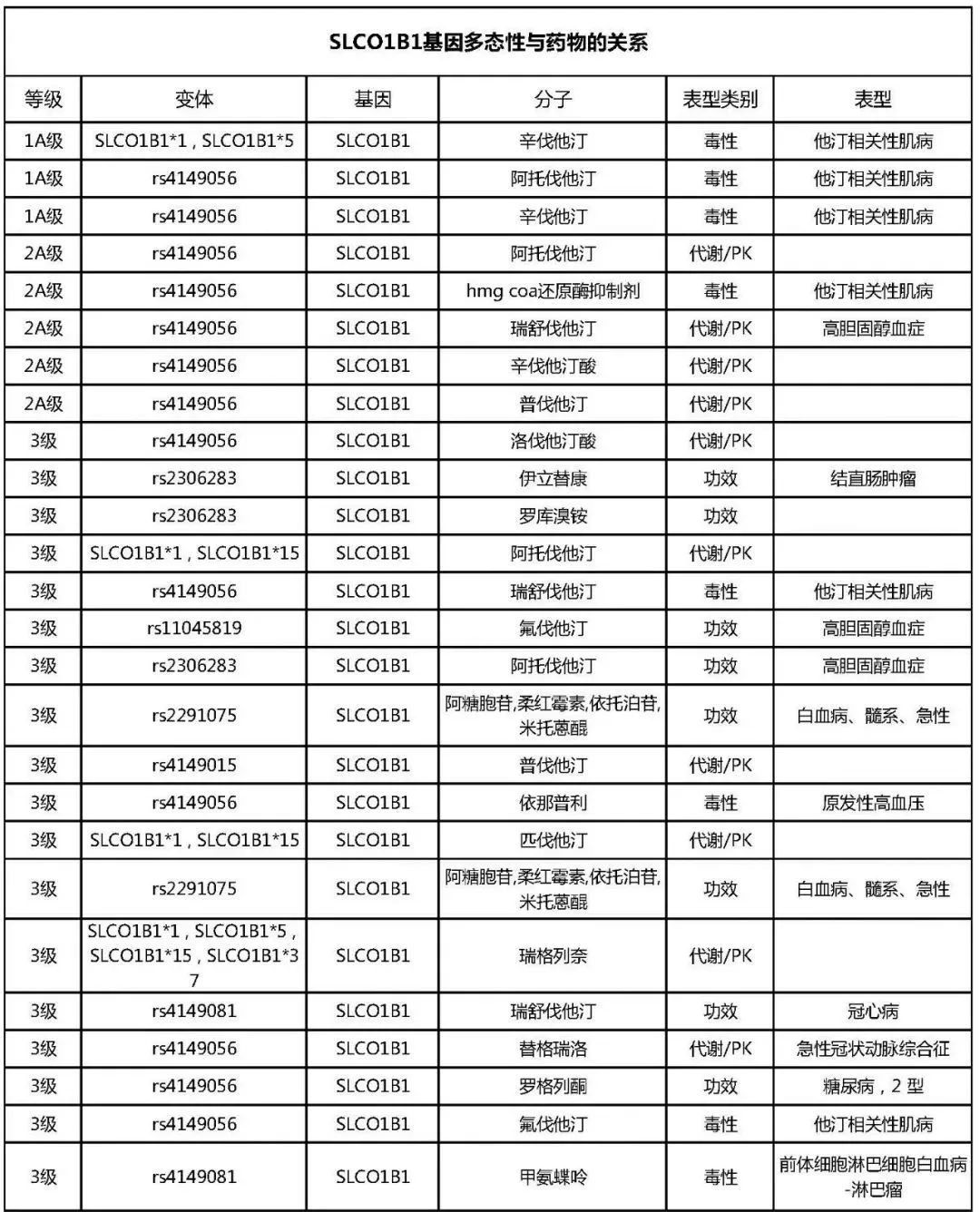
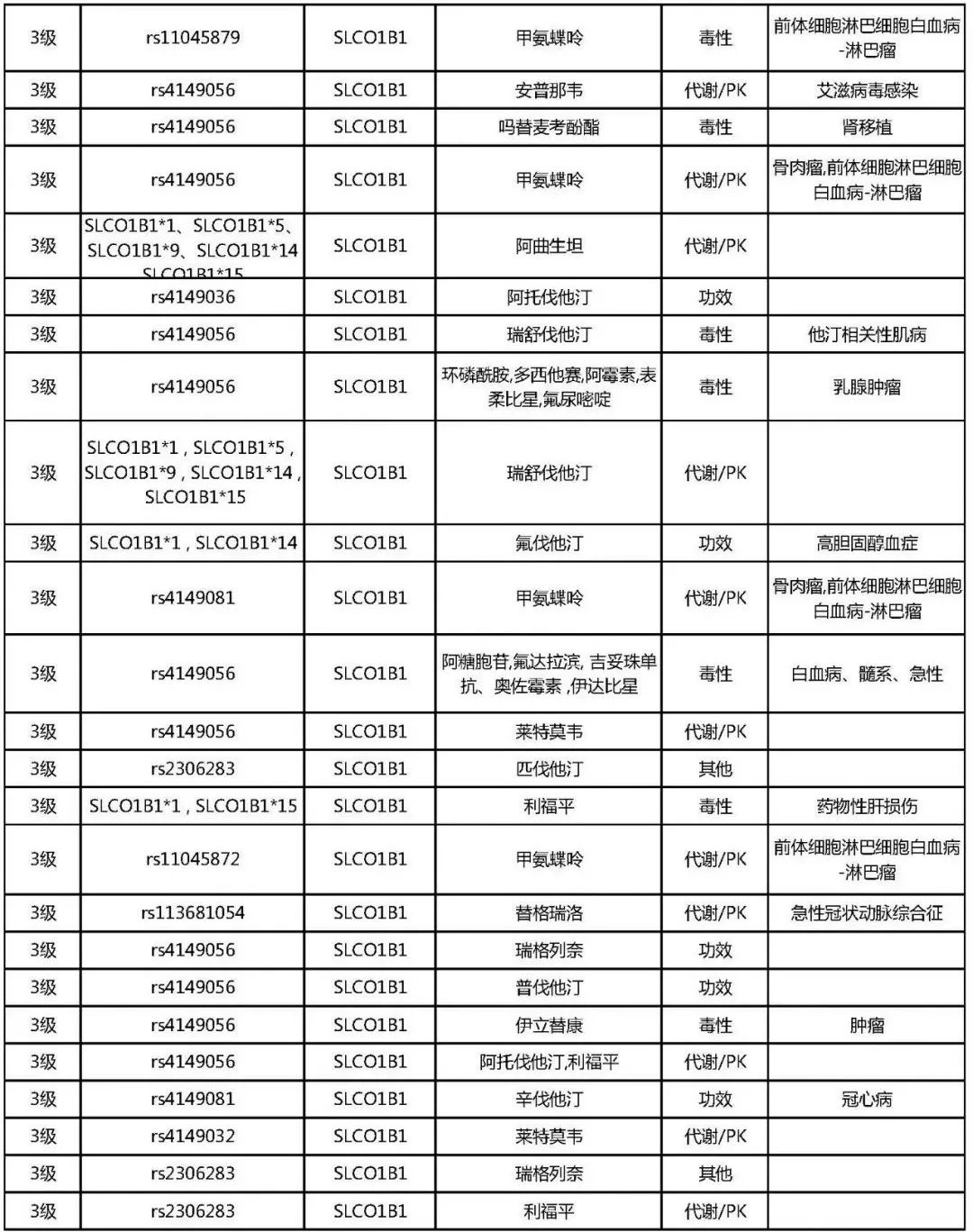
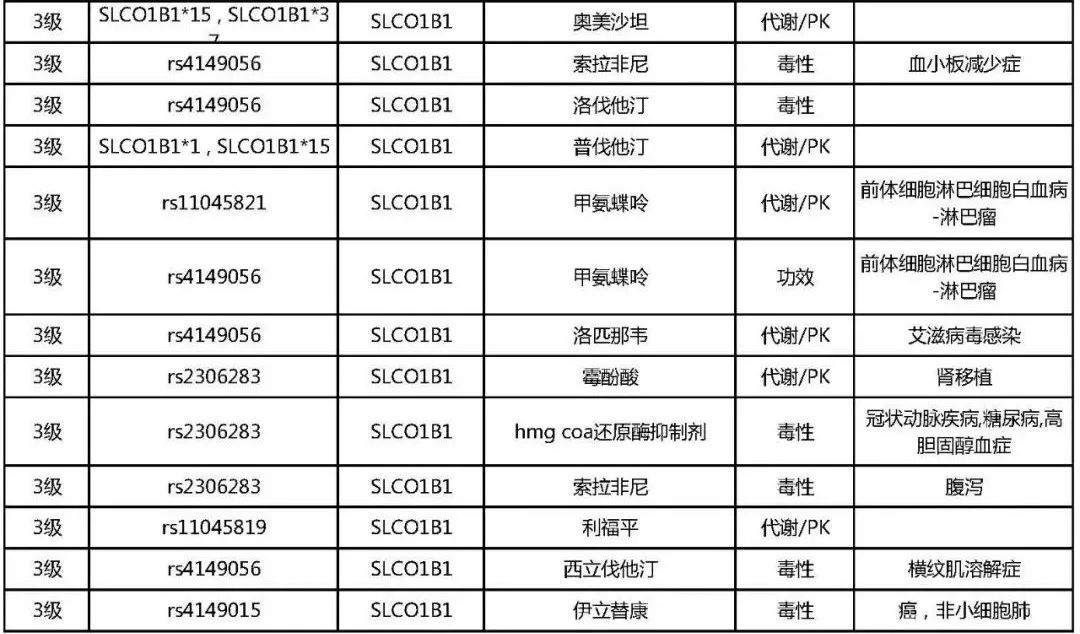

总结
大量的生物医学研究成果表明,绝大部分的药物反应个体差异是由遗传因素造成的。据联合国世界卫生组织统计,全球死亡患者中,三分之一是死于不合理用药,而非死于自然疾病本身。药物不良反应成为除了癌症,脑溢血和心脏病外的第四大死因,由此可见,安全用药已成为世界性的公共医疗卫生问题。
个体化治疗(Individualized Drug Therapy)是以每个患者的信息为基础决定治疗方案,从基因多态性的差异来把握治疗效果或毒副作用等应答的特性,对每个患者进行最适宜的治疗方案。FDA和NIH正在大力推进转化医学和个体化医疗。世界卫生组织(WHO)已明确指出:21世纪的医学将从疾病医学向健康医学发展,从群体治疗向个体治疗发展。
所以基因在未来的诊疗过程中将具有越来越重要的地位。未来就诊革新的趋势是在诊疗过程中加强对于患者的基因信息的收集及分析的力度。在传统的病理信息(血液指标、影像学信息、表观指征信息等)的基础上,将基因信息加入到病例之中进行个体化的用药指导。区域基因数据的大规模收集,将使药物的个体化建议更加准确。而基因区域分布频率的完善,可以对于区域的高发疾病预防提供更精准的方案。
参考文献:
[1]. Group H . HPS2-THRIVE randomized placebo-controlled trial in 25 673 high-risk patients of ER niacin/laropiprant: trial design, pre-specified muscle and liver outcomes, and reasons for stopping study treatment[J]. European Heart Journal, 2013(17):1279-1291.
[2]. Joseph K , Eduard M , Anees D , et al. Pharmacogenomics of statins: understanding susceptibility to adverse effects[J]. Pharmacogenomics & Personalized Medicine, 2016, 9:97-106.
[3]. Elena A , Marzia D R , Leonardo F , et al. Pharmacogenetic Foundations of Therapeutic Efficacy and Adverse Events of Statins[J]. International Journal of Molecular Sciences, 2017, 18(1).
[4]. Niemi M , Pasanen M K , Neuvonen P J . Organic anion transporting polypeptide 1B1: a genetically polymorphic transporter of major importance for hepatic drug uptake.[J]. Pharmacological Reviews, 2011, 63(1):157-181.
[5]. Pharmacogenetic meta-analysis of genome-wide association studies of LDL cholesterol response to statins[J]. Nature Communications.
[6]. Rachel D , Sivan B A , Dror H , et al. ApoE Genotype, Lipid Profile, Exercise, and the Associations With Cardiovascular Morbidity and 18-Year Mortality[J]. The Journals of Gerontology: Series A, 2019(10):10.
[7]. 宁昕, 邱龄. 载脂蛋白E基因多态性与他汀类药物降脂疗效的关系[J]. 中国循证心血管医学杂志, 2018, 10(9):4.
[8]. CPIC指南
[9]. PharmGKB数据库




